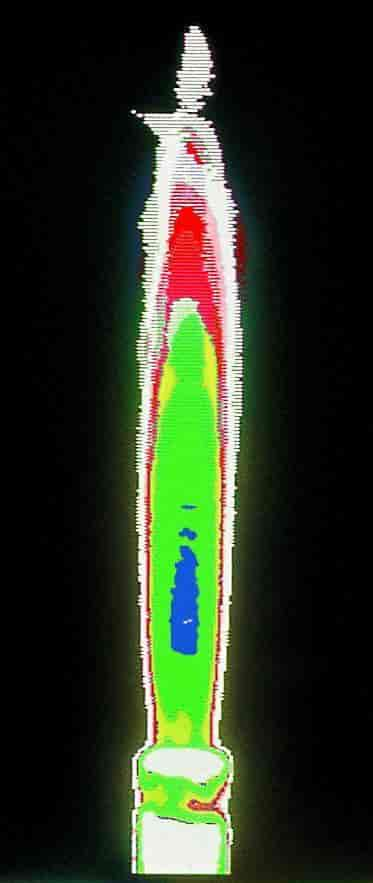
Flamme, synlig, dvs. lysende, forbrænding af gas. I stærkt lysende flammer kommer lyset fra glødende kulpartikler, som dannes ved den termiske nedbrydning af gassens kulstofforbindelser, fx methan i naturgas og propan i flaskegas. Flammens farve er gul. Hvis gassen blandes med en passende luftmængde umiddelbart før forbrændingen som i bunsenbrændere, vil forbrændingens mellemtrin, kulstofdannelsen, næsten udeblive og flammen kun lyse svagt med blå farve. Ren brint (hydrogen) brænder ligeledes med svagt lysende blå flamme.
Faste brændsler som træ og kul brænder også med lysende flamme, hvilket skyldes, at brændslet ved opvarmning afgiver gasformige kulstofforbindelser. Hvis det faste brændsel ikke kan afgive gas, hvilket gælder fx trækul og koks, brænder det uden flammer, men det ophedede brændsel gløder med rød eller gul farve.
Flammer kan have en intens farve, hvis brændslet indeholder salte af visse metaller. Natrium giver en stærk gul farve, som let dominerer over farver fra andre bestanddele. Barium og lithium giver henholdsvis grøn og rød flammefarve. Disse forhold udnyttes ved fremstilling af fyrværkeri.




Kommentarer
Kommentarer til artiklen bliver synlige for alle. Undlad at skrive følsomme oplysninger, for eksempel sundhedsoplysninger. Fagansvarlig eller redaktør svarer, når de kan.
Du skal være logget ind for at kommentere.