Nernsts ligning, i elektrokemien en ligning, der beskriver sammenhængen mellem en elektrodes elektriske potential og koncentrationerne af de kemiske reaktanter i et galvanisk element. Ligningen udtrykkes ved
Faktaboks
- Etymologi
- Ligningen er opkaldt efter den tyske kemiker Walther Nernst.
hvor E er det elektriske potential af elektroden, E0 er normalpotentialet, R er gaskonstanten, T er den absolutte temperatur (i kelvin), n er antallet af elektroner, der omsættes pr. gennemløb af den elektrokemiske proces, F er Faradays konstant, og aox og ared er produktet af de kemiske aktiviteter (se aktivitet) af hhv. de oxiderede og de reducerede reaktanter.
Ligningen gælder, når elektroden er i ligevægt, dvs. når der ikke trækkes strøm fra elementet. I vandige elektrolytter med lave koncentrationer af reaktanterne kan aktiviteterne sættes lig med koncentrationerne. I tilfælde af gasformige reaktanter er aktiviteterne lig med partialtrykkene.


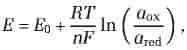


Kommentarer
Kommentarer til artiklen bliver synlige for alle. Undlad at skrive følsomme oplysninger, for eksempel sundhedsoplysninger. Fagansvarlig eller redaktør svarer, når de kan.
Du skal være logget ind for at kommentere.